不同等级洁净区悬浮粒子、浮游菌微生物检测有哪些要求?
2025-03
基于 2025年02月25日 现行 GMP(药品生产质量管理规范) 和 ISO 14644/ISO 13408 标准的详细要求,涵盖洁净区悬浮粒子、浮游菌的检测方法、频率及关键操作细则分享。
1. 悬浮粒子监测
2. 浮游菌监测
3.洁净等级与检测参数总表
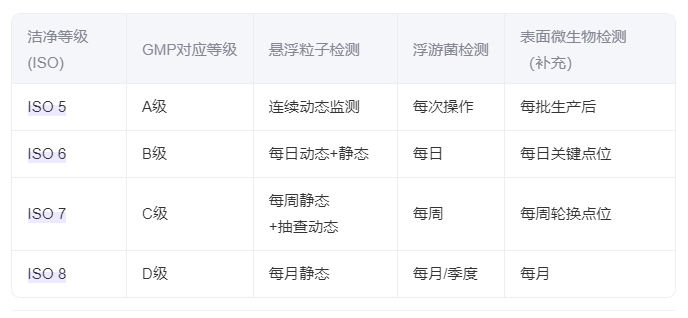
-
- 标准依据:ISO 14644-1(分级)、GMP附录1(动态控制)。
- 粒径范围:≥0.5μm和≥5μm(A/B级需同时监测)。
- 采样点数量:
- ISO 5/A级:至少每分钟采样1次,覆盖所有操作点位(如灌装线、工作台)。
- 设备校准:粒子计数器需符合ISO 21501-4,每年第三方校准。
- 采样高度:工作平面高度(通常离地0.8-1.2m)。
- 数据记录:需保存原始数据并计算UCL(95%置信上限)用于合规判定。
1. 检测标准与方法
- 标准依据:ISO 13408-6(无菌工艺)、GMP附录1。
- 采样器类型:撞击式(如MAS-100NT)或离心式(需验证捕获效率≥50%)。
- 培养基:胰酪大豆胨琼脂(TSA),培养条件:20-25℃(3天)+30-35℃(2天)。
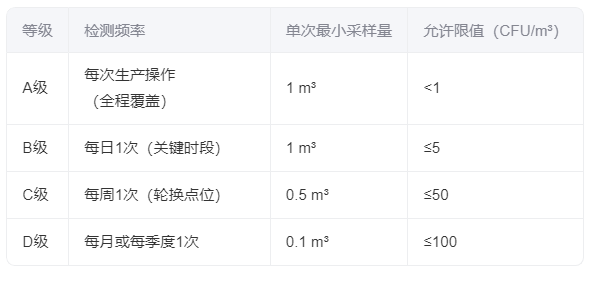
2. 频率与采样量
3. 注意事项
- 无菌操作:采样前对采样头进行酒精或蒸汽灭菌。
- 采样时间:避免人员走动高峰期,采样时长不超过4小时。
- 超标处理:若B级区超标,需扩大采样范围并评估产品污染风险。
-
- 标准依据
- 悬浮粒子:ISO 14644-1 规定粒径阈值(如≥0.5μm和≥5μm),GMP要求动态监测且数据实时记录。
- 浮游菌:GMP附录1强调采样点需覆盖高风险区域(如灌装线、敞口容器上方)。
-
- 特殊场景
- 无菌生产A级区:浮游菌监测宜采用便携式设备,避免人员频繁进出。
- 停产重启:需完成完整的静态与动态环境确认。















