北京中邦兴业作为一家专业为生物制药、集成电路、芯片、半导体、新能源等行业提供洁净环境整体解决方案的服务商,为客户提供了大量的仪器设备和服务工程。中邦将持续深耕洁净产业,加大研发投入,生产更高端、更高品质的洁净环境检测仪器设备,助力洁净产业的健康发展,为不同行业,拥有洁净环境监测需求的客户,提供一站式的解决方案,助力洁净产业持续健康发展。

>一个喷嚏可以射出100,000-1,000,000个微生物
>健康人群也向环境中散布颗粒(例如人体的脱落物:)
>站着不动也可以每分钟散布100,000个颗粒,移动时数量会猛增
人是最大的污染源!

·正确的更衣和洗手
·正确的洁净室操作行为
·人员健康
.外来人员管理
培训应包括理论和现场的指导
先进行非关键操作
通过培养基模拟灌装试验对员工进行考核
没有经过资质确认的人员
在有资质的人员指导下更衣以及在无菌生产洁净区内的活动
其退出洁净区前对其进行取样
对其所经过的区域进行必要的消毒

2、洁净区的动态监测悬浮粒子的动态监测
关键操作的全过程,对A级区进行粒子监测
A级区的监测频率、取样量,及时发现人为干预、偶发事件及任何系统的破坏
B级区:类似于A级区,采样频率、采样量可以调整
C级区:质量风险管理原则确定
D级区:一般不作要求,( 法规 : 必要时 )
对于C/D级区的自净时间应达到规定要求
取样量和取样点
ISO14644-1 B.4.2 节有明确的采样量的计算公式采样量(升)=(20/级别中最大粒子限度)x1000,显然对于A 级,采样量为(20/20)x1000 =1米3从上式中可见,级别要求越低,取样量就越小
取样点数由B.1.1公式取样点数 NL =,A为洁净区面积,例如10米x5米的区域,取样点应为8(取整数)取样点均匀分布,位于工作面高度
注意: 这里仅指在洁净区划分时加以采用
悬浮粒子的动态监测常用仪器
微生物的要求:附录1<无菌药品> 第十一条监测方法有:
1)、空气浮游菌监测
沉降菌法–被动法
>沉降碟在空气中的暴露时间<4小时
>监控整个灌装过程
>只能给出定性和半定量的数据
>应结合空气浮游菌的数据,对沉降碟的结果进行评价定量空气
定量空气浮游菌采样法–主动法
>撞击式,离心式和膜过滤( 明胶 ) 取样仪
应取一定体积的空气( 取样体积应有代表性)
>仪器应经过校验
定量空气浮游菌采样常用仪器-撞击式
2)、环境表面监测表面取样法(如棉签擦拭法和接触碟法)
3)、人员监测表面取样法(接触碟法)
>表面取样法( 接触碟法),取样时间一般为
>工作结束,离开洁净区前取样
>处理异常情况后(取样后重新更衣或更换手套)
>生产过程中随时监测
特别注意:
>不得在刚消毒过后取样


取样计划的影响因素:产品类型、生产过程、设施/工艺设计、生产密度、人为千扰、环境监测历史数据等
取样点的选择主要取决于洁净室的设计和生产要求
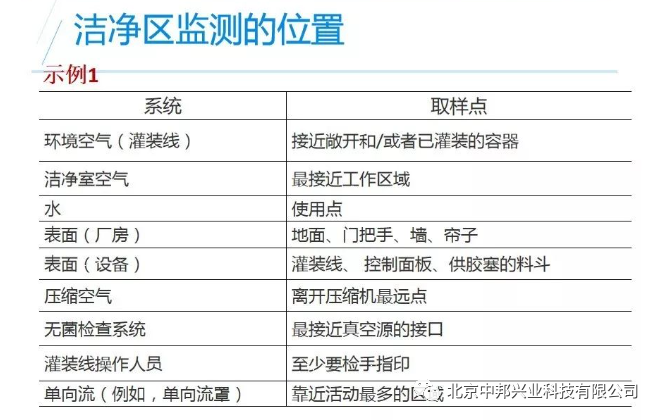

在生产过程中,什么地点最容易长菌 ?
哪些地方是清洁、消毒或灭菌时最难覆盖/接触或最难奏效的部位 ?
什么活动会导致污染的扩散 ?
在某一部位的取样操作,足以导致测试数据的差错或污染产品 ?取样只应在生产结尾换班时进行吗?


如果您有关于无菌药品生产质量管理,环境监测方面的问题,可以直接扫描北京中邦兴业公众号二维码,专业技术工程师为您一对一解答。















